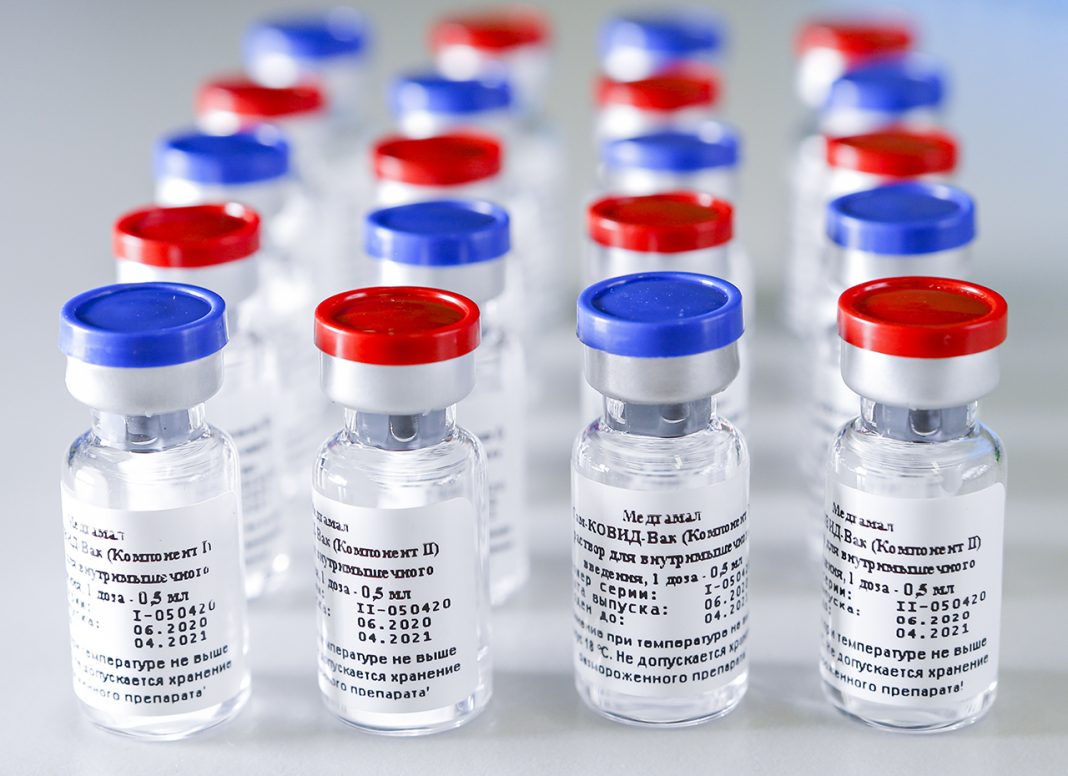
Разработчики вакцины против коронавирусной инфекции «Спутник V» меняют методы оценки препарата, рассчитывая на его более легкую регистрацию в Европейском агентстве лекарственных средств (ЕМА). Об этом пишет ТАСС со ссылкой на и. о. генерального директора ФГБУ «Научный центр экспертизы средств медицинского применения» Минздрава России Валентину Косенко.
«Сегодня, когда идет регистрация в Европейском агентстве [лекарственных средств] «Спутника V», то некоторые методы, еще использующиеся в России для оценки качества лекарственных препаратов, не принимаются в разных более развитых странах по фармацевтике и, в частности, в Европе. Так, разработчики «Спутника V» сегодня ведут работу по замене методов, ведущихся на животных методами in vitro», – сказала Косенко во время форума «Биотехмед».
EMA до сих пор не разрешило использование «Спутника V» в Евросоюзе. Позиция Еврокомиссии в отношении российской вакцины неизменна с начала июля, когда заработала система ковид-сертификатов ЕС. У государств сообщества, использующих «Спутник V» (например, у Венгрии), есть право на выдачу на него европейских цифровых сертификатов вакцинации, но остальные страны ЕС могут по собственному усмотрению принимать или нет эти документы.
«Спутник V» зарегистрировали в России 11 августа 2020 года. Он стал первой в мире официально зарегистрированной вакциной от COVID-19.
Глава Минздрава РФ ранее заявил о снятии всех барьеров для признания «Спутника V» в ВОЗ.